Em continuidade ao programa de amostragens de longo prazo em andamento desde 1992, amostras de água de superfície serão obtidas mensalmente para medidas de Clorofila a, contagem de células e medidas de parâmetros físicos e químicos (temperatura, salinidade e nutrientes inorgânicos dissolvidos: amônia, nitrito+nitrato, fosfato e silicato – Strickland & Parsons, 1973) em três estações fixas, sendo duas localizadas no estuário e uma na zona de arrebentação da praia oceânica adjacente (1. estuário médio, trapiche do Yacht Club de Rio Grande; 2. desembocadura, trapiche da Prainha na 4ª secção da Barra; 3. praia Cassino, em frente a Estação de Aquacultura (EMA; Fig. 1). Nestas mesmas estações, serão também obtidas amostras de rede de plâncton (cônica, 22μm de malha) para a identificação dos organismos. Os organismos serão contados ao microscópio invertido (Sournia 1978) e sua identificação dar-se-á em microscópio ótico de luz transmitida e, quando necessário, com utilização de microscopia eletrônica. As concentrações de clorofila a e de feopigmentos serão determinadas fluorimetricamente (Welschmeyer 1994). Concomitantemente às amostragens bióticas, serão medidas in situ a temperatura e salinidade com termosalinômetro YSI (Mod. 33 SCT) e profundidade do disco de Secchi.
|
Estação de coleta 1 |
Estação de coleta 2 |
|
Estação de coleta 3 |
Floração de diatomáceas na praia |
|
Análise em laboratório |
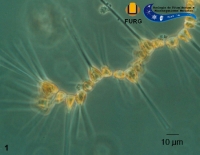
Asterionellopsis glacialis |
Serão ainda realizadas análises de pigmentos do fitoplâncton. Para tal, amostras de água serão filtradas em filtros de fibra de vidro (GF/F 25 mm de diâmetro) e armazenadas em ultrafreezer até análise. A extração dos pigmentos será realizada utilizando-se uma solução padrão de metanol 95% tamponado, e adição de um reagente padrão interno (utilizado para verificar a otimização da extração). Os filtros
são macerados e mantidos em freezer, seguido de um banho frio de ultrassom. Após centrifugação refrigerada, a amostra é filtrada (0,2 μm) e imediatamente inserida no auto-injetor do HPLC. O instrumento é composto por um módulo distribuidor de solventes, um sistema de controle, um detector de fotodiodos e um detector de fluorescência. A separação cromatográfica dos pigmentos é efetuada usando uma coluna C8 monomérica. A fase móvel (solventes) e o seu respectivo gradiente segue o método desenvolvido por Zapata et al. (2000),
discutido e otimizado por Mendes et al. (2007). Os picos referentes aos pigmentos fotossintéticos serão identificados e quantificados com base em padrões comerciais da DHI (Institute for Water and Environment, Denmark). A concentração é calculada a partir do sinal obtido pelo detector de fotodiodos e/ou pelo detector de fluorescência, para o caso dos pigmentos clorofilianos. As comunidades de fitoplâncton são identificadas em seus pigmentos "diagnósticos" utilizando-se o programa estatístico CHEMTAX (versão 1.95), que utiliza um processo interativo de fatorização matricial para otimizar a associação entre os diferentes pigmentos presentes (e razões entre os pigmentos típicos e a clorofila a) e a composição dos grupos taxonômicos (Mackey et al. 1996). É necessário partir de uma matriz de entrada
de razões entre pigmentos, que seja o mais próximo possível da matriz 'esperada', de acordo com as espécies e grupos presentes na amostra. Após otimização da matriz e considerando as concentrações e razões pigmentares, é possível estimar a abundância de cada classe de fitoplâncton presente e a sua contribuição para o total de clorofila a (índice de biomassa).